Ngay từ khi những loại vaccine đầu tiên trên thế giới được phát minh, bên cạnh tiêm chủng cho người lớn thì các quốc gia đã bắt tay vào thử nghiệm tiêm vaccine (kể cả chủng virus bất hoạt, hay MRA) trên đối tượng học đường (12 - 18 tuổi). Tới nay, đã có một số kết quả nghiên cứu nhất định.
PFIZER
Hồi tháng 3, Pfizer cho biết các thử nghiệm lâm sàng cho thấy vaccine của hãng an toàn và hiệu quả 100% ở trẻ em 12 - 15 tuổi, so với hiệu quả 95% ở người lớn tham gia thử nghiệm. Các chuyên gia ghi nhận 18 trường hợp nhiễm nCoV có triệu chứng ở nhóm dùng giả dược, không trường hợp nào mắc bệnh ở nhóm tiêm vaccine. Vaccine cũng an toàn, tác dụng phụ với trẻ em tương đương với người lớn.
FDA phê duyệt khẩn cấp vaccine Pfizer ở người từ 12 đến 15 tuổi, đồng thời mở rộng thử nghiệm ở nhóm từ 5 đến 11 tuổi. Hãng đã gửi dữ liệu nghiên cứu đến FDA hồi cuối tháng 9 để xin cấp phép khẩn cấp. Theo đó, vaccine tạo phản ứng kháng thể mạnh mẽ và an toàn với người dùng. Hãng sẽ thông báo số liệu cụ thể trong cuộc họp với FDA sắp tới.
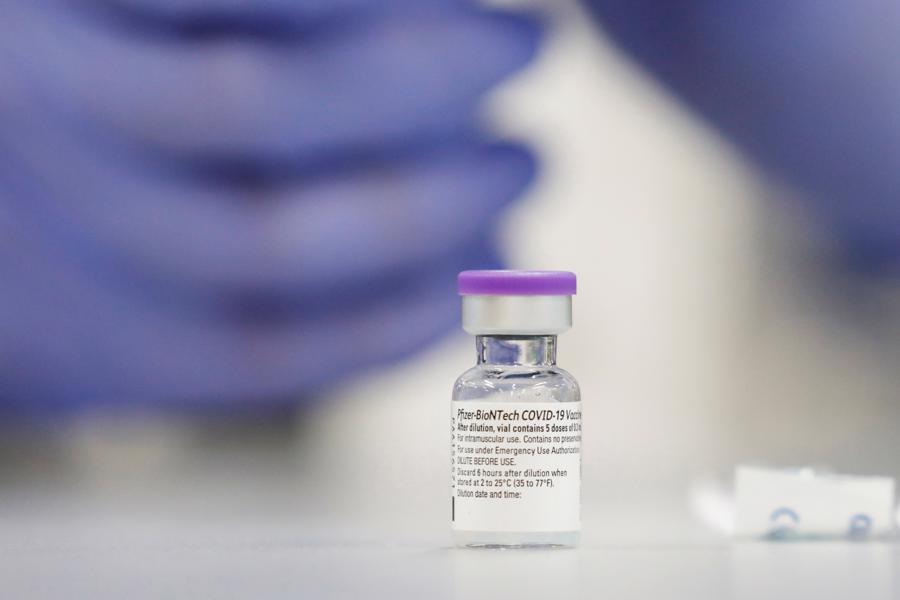
Hơn 2.200 tình nguyện viên 5 - 11 tuổi được tiêm theo liệu trình hai liều vaccine 10 microgam, nhỏ hơn so với liều 30 microgam được dùng ở nhóm 12 tuổi trở lên. Công ty cho biết liều lượng này "được lựa chọn cẩn thận dựa trên tính an toàn, khả năng dung nạp và sản sinh miễn dịch".
Trong thử nghiệm lâm sàng dành cho trẻ dưới 5 tuổi, Pfizer sử dụng liều 3 microgram. Hãng dự kiến thông báo kết quả ở nhóm này sớm nhất là vào quý 4 năm nay.
MODERNA
Theo thử nghiệm lâm sàng công bố trên Tạp chí Y học New England hồi tháng 8, vaccine an toàn, có hoạt tính mạnh mẽ chống lại nCoV ở người từ 12 đến 15 tuổi. Trong phân tích ban đầu, vaccine hiệu quả khoảng 93,4% sau hai liều, ngăn ngừa 100% ca nhập viện và tử vong. Phản ứng phụ là đau tại vùng tiêm, nhức đầu, mệt mỏi, ớn lạnh và đau cơ. Các triệu chứng kéo dài trung bình 4 ngày. Không có trường hợp nào tử vong hoặc biến chứng không mong muốn.
Trước đó, Moderna đã yêu cầu FDA cho phép sử dụng khẩn cấp vaccine ở người từ 12 đến 17 tuổi. Kết quả mới nhất bổ sung thêm dữ liệu cho thử nghiệm lâm sàng giai đoạn 2/3 công bố hồi tháng 5. Nếu được chấp thuận, đây sẽ là loại vaccine thứ hai tại Mỹ sử dụng cho thanh thiếu niên, bên cạnh Pfizer.
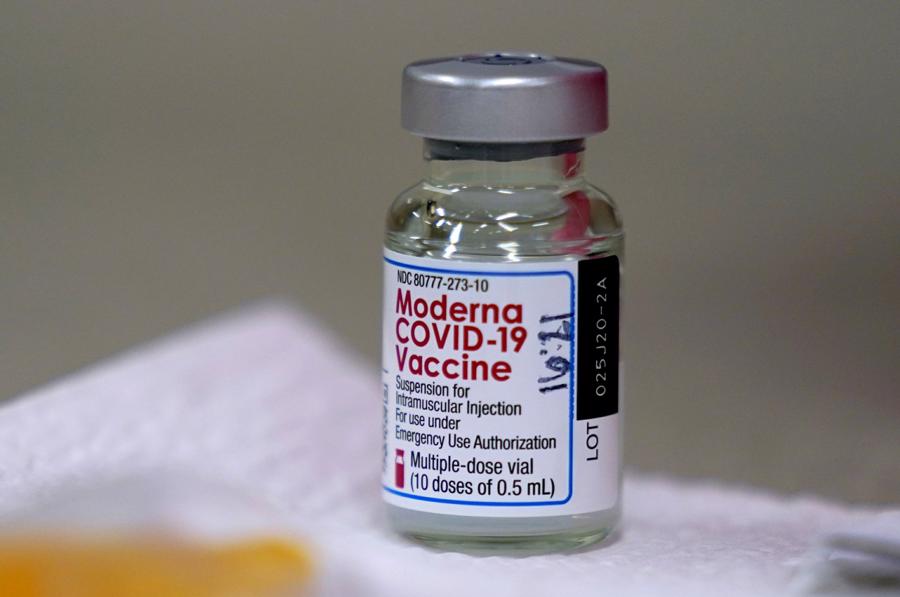
Tại châu Âu, Moderna đã được phê duyệt cho trẻ từ 12 đến 17 tuổi. Cơ quan Dược phẩm châu Âu nghiên cứu vaccine với hơn 3.700 trẻ, ghi nhận phản ứng kháng thể tương đương với người trưởng thành. Tác dụng phụ ở trẻ em cũng giống với người lớn, tiêu biểu là mệt mỏi, nhức đầu, đau cơ và khớp...
Đến tháng 8, Moderna thông báo khởi động thử nghiệm ở trẻ từ 6 tháng đến 12 tuổi, có khoảng 7.000 tình nguyện viên tham gia. Các chuyên gia có cái nhìn lạc quan, cho rằng vaccine Moderna sẽ hiệu quả tương đương ở nhóm này.
JOHNSON & JOHNSON
Hồi tháng 9, hãng này thông báo kế hoạch thử nghiệm giai đoạn ba vaccine cho trẻ nhỏ, song không cung cấp thời gian cụ thể. Nghiên cứu giai đoạn một và hai đã kết thúc, tuy nhiên chưa có dữ liệu chính thức.
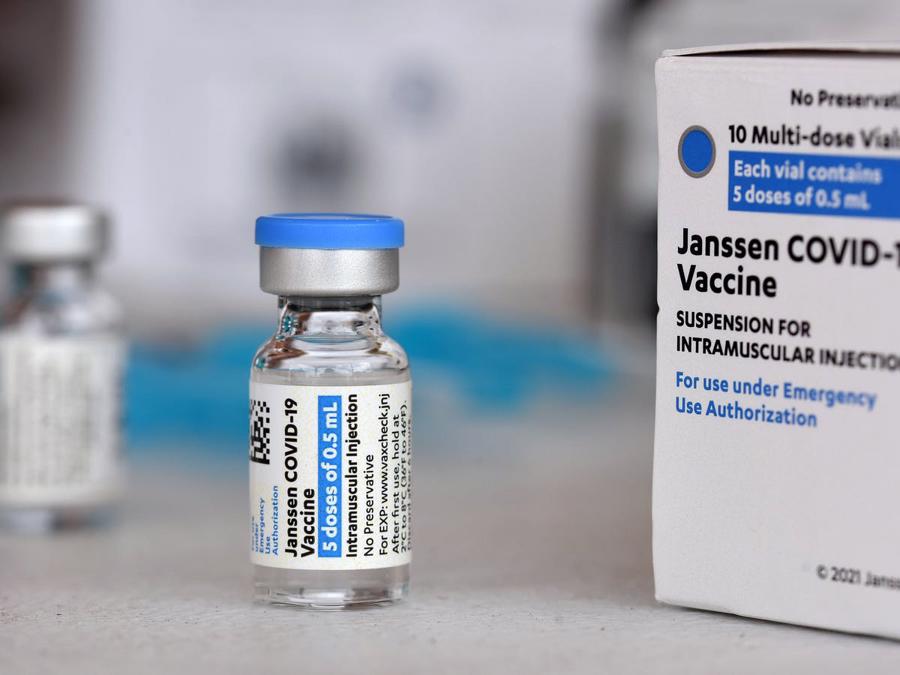
Phó giáo sư Maureen Ferran tại Viện Công nghệ Rochester, Mỹ, cho biết khởi đầu chậm trễ khiến hãng dược này gặp bất lợi đôi chút so với các nhà sản xuất vaccine mRNA. "Hiện vaccine chưa được chấp thuận ở trẻ dưới 18 tuổi, chưa hoàn thành thử nghiệm. Có vẻ phải đến năm 2022, vaccine mới được xem xét phê duyệt (tại Mỹ)", ông nói.
SINOPHARM
Tháng 9, Sinopharm công bố dữ liệu mới cho thấy vaccine Covid-19 của hãng an toàn đối với trẻ em từ 3 tuổi trở lên. Kết quả thử nghiệm lâm sàng giai đoạn 1 và 2 được công bố trên tạp chí The Lancet Infectious Diseases cho thấy, vaccine do Sinopharm phát triển an toàn đối với trẻ tham gia thử nghiệm 3 - 17 tuổi.
Trong thử nghiệm, loại vaccine này cho thấy phản ứng miễn dịch mạnh mẽ ở trẻ em và lượng kháng thể trung hòa tương tự như ở người lớn. Nghiên cứu được thực hiện tại tỉnh Hà Nam, trong đó giai đoạn 1 có 288 trẻ em tham gia, giai đoạn 2 có 720 trẻ em. Tác dụng phụ xuất hiện chủ yếu từ nhẹ đến trung bình, có một trường hợp phản ứng nghiêm trọng là trẻ có tiền sử dị ứng thực phẩm.
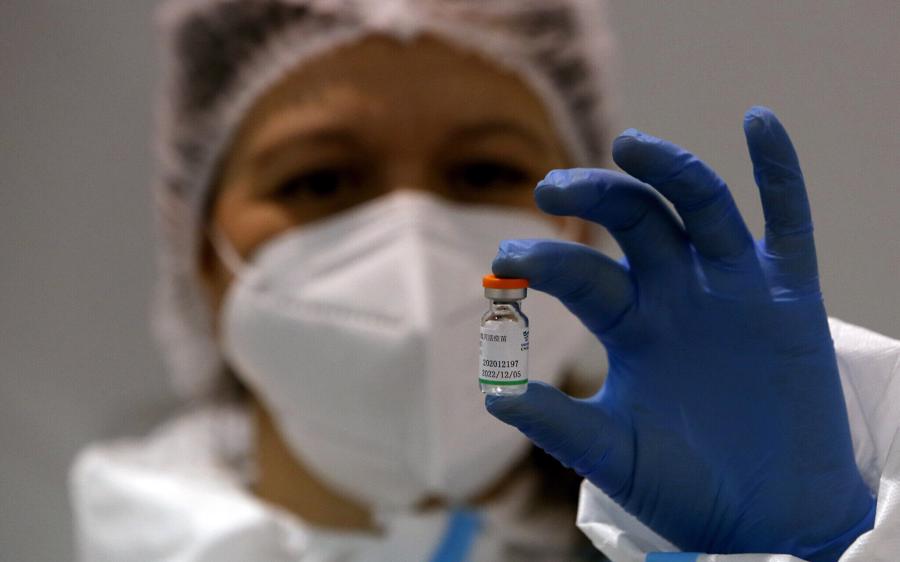
Trung Quốc đã cấp phép sử dụng khẩn cấp vaccine của hai hãng Sinopharm và Sinovac cho trẻ em từ 3 - 17 tuổi, nhưng đến nay mới chỉ giới hạn cho trẻ từ 12 tuổi trở lên. Theo Bộ Giáo dục Trung Quốc, nước này hiện đã tiêm chủng đầy đủ cho 91% trẻ em ở độ tuổi từ 12 - 17.
ASTRA ZENECA
Hãng dược AstraZeneca đang khởi động thử nghiệm vaccine ở trẻ em và thanh thiếu niên từ 6 đến 17 tuổi. Mục tiêu là đánh giá tính an toàn và phản ứng miễn dịch ở nhóm tuổi này. Thử nghiệm dự kiến có 300 tình nguyện viên, diễn ra tại Oxford, Southampton, London và Bristol.
Trẻ em tham gia thử nghiệm được tiêm vaccine AstraZenca (liều tương tự người lớn) hoặc vaccine viêm màng não làm giả dược. Sau đó, các em và gia đình điền vào sổ sức khỏe điện tử trong 28 ngày để theo dõi triệu chứng, đồng thời được xét nghiệm máu trong suốt quá trình nghiên cứu để kiểm tra phản ứng miễn dịch.
MỘT SỐ VACCINE KHÁC
Trung Quốc đang thử nghiệm lâm sàng pha 1/2 vaccine Verocells ở trẻ 3 - 17 tuổi. Kết quả cho thấy, vaccine an toàn và tạo ra đáp ứng miễn dịch khi tiêm đủ 2 liều. Vaccine này chưa được phê duyệt sử dụng cho trẻ em vì chưa có kết quả thử nghiệm pha 3.
Vaccine Covaxin (Ấn Độ) hiện cũng đã hoàn thành thử nghiệm pha 2/3 cho trẻ 2 - 18 tuổi nhưng chưa có công bố trên báo khoa học.
Cho đến nay, các vaccine khác cũng đang tiến hành thử nghiệm trên trẻ nhỏ là Novavax của Mỹ, Covaxin xịt mũi của Ấn độ, và Sputnik xịt mũi của Nga.
Hiện mới có thông tin về tác dụng phụ ngắn hạn của mRNA vaccine. Tác dụng phụ sau tiêm phổ biến là đau và sưng chỗ tiêm, mệt mỏi, nhức đầu, đau cơ, sốt, có thể buồn nôn và sẽ tự hết sau vài ngày.
Trung tâm kiểm soát và phòng ngừa dịch bệnh (CDC) Hoa Kỳ đã nhận được các báo cáo về các trường hợp viêm cơ tim sau tiêm vaccine Pfizer hoặc Moderna, nhưng tỷ lệ mắc rất thấp và ở mức độ nhẹ. Đối với Pfizer, tỷ lệ mắc viêm cơ tim sau tiêm vaccine là 162 người mắc trong 1 triệu bé trai 12 - 15 tuổi và 94 người trong 1 triệu bé trai 16 - 17 tuổi được tiêm vaccine. Tỷ lệ này cao hơn sau khi tiêm mũi 2 vaccine Pfizer, thường xuất hiện trong vòng 1 tuần đầu sau tiêm mũi 2.













 Google translate
Google translate